Wissen aus dem Bereich Medizintechnik
Der Wissensbereich Medizintechnik gibt Ihnen einen Überblick über die wichtigsten Änderungen der Aktualisierung der DIN EN ISO 13485. Darüber hinaus finden Sie Informationen zu den Themen Validierung manueller Prozesse und Lieferantenmanagement.
Hier finden Sie Antworten auf die folgenden Fragen:
- Welche Änderungen brachte die Aktualisierung der DIN EN ISO 13485?
- Müssen manuelle Prozesse in der Medizintechnik validiert werden?
- Was ist ein Design History File und was muss bei der Erstellung beachtet werden?
- Wie kann ein effizientes Lieferantenmanagement bei der Qualitätssicherung von ausgelagerten Prozessen aufgebaut sein?
Welche Änderungen brachte die Aktualisierung der DIN EN ISO 13485?
Auszug aus den wichtigsten Änderungen der neuen DIN EN ISO 13485:
- Zusätzliche regulatorische Anforderungen in den Bereichen Validierung, Verifizierung, Design und Entwicklung
- Risikomanagement wird innerhalb des Qualitätsmanagementsystems stärker berücksichtigt
- Forderung nach Software-Validierung wird deutlicher herausgestellt
Müssen manuelle Fertigungsprozesse in der Medizintechnik validiert werden?
Gemäß den regulatorischen Vorgaben der ISO Norm 13485 und den Quality System Regulations der FDA bedürfen Prozesse, deren Prozessergebnisse nicht (ausreichend) verifiziert werden oder verifiziert werden können, der Validierung - unabhängig davon, ob der Prozess manuelle Tätigkeiten umfasst. Manuelle Prozesse müssen daher genau so betrachtet werden wie automatisierte Prozesse.
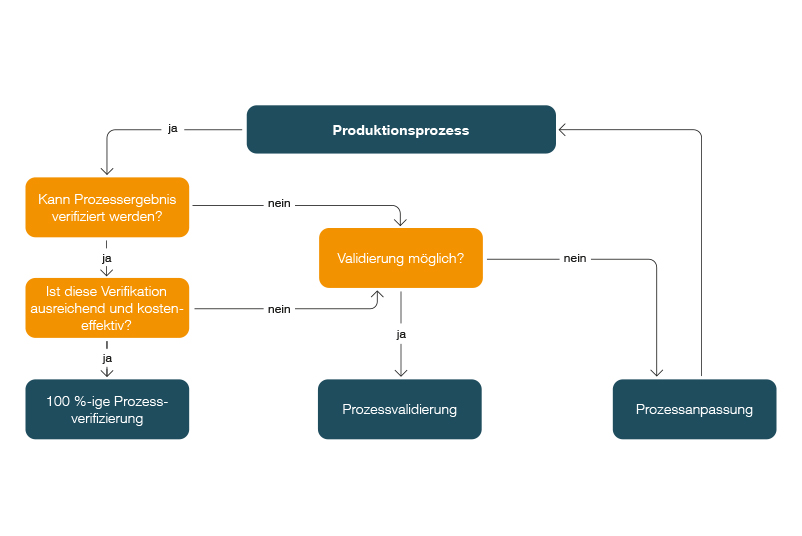
Validierung manueller Prozesse in der Medizintechnik
Es ergibt sich folgender Entscheidungsbaum zur Festlegung, ob ein Prozess validiert werden sollte:
Was ist ein Design History File und was muss bei der Erstellung beachtet werden?
Der Design-History-File (DHF) stellt eine Aufzeichnung der Entwicklungsgeschichte und der Entwicklungsergebnisse eines Medizinproduktes dar. Konkret sind u. a. zu dokumentieren:
- Einsatzzweck des Produktes (Intended Use)
- Anforderungen und ihre Detaillierung mit Spezifikationen
- Designbeschreibung und Funktionsweise
- Konstruktionszeichnungen
- Testpläne für die Designverifizierung
- Testpläne für die Designvalidierung
Erfahren Sie mehr zum Thema bei einer unserer Erfolgsgeschichten:
Wie kann ein effizientes Lieferantenmanagement bei der Qualitätssicherung von ausgelagerten Prozessen aufgebaut sein?
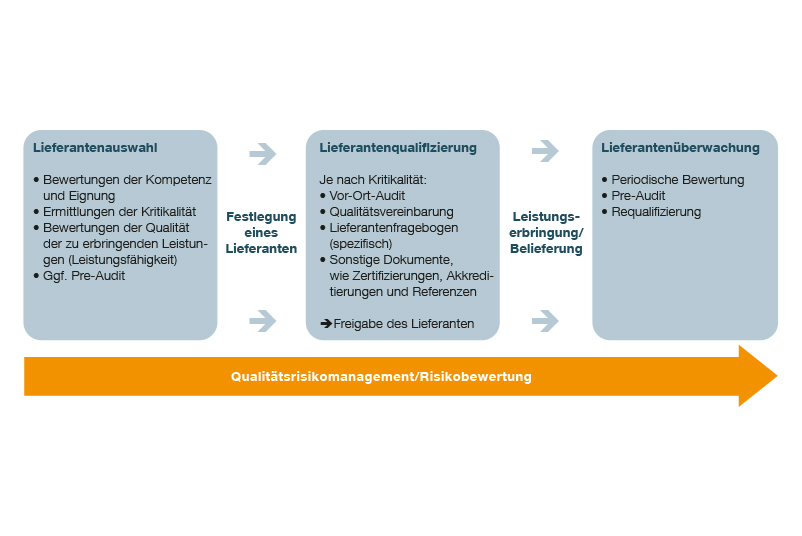
Praktisch kann das Lieferantenmanagement mehrstufig aufgebaut werden und folgende Schritte umfassen:
- Bewertungskatalog zur Lieferantenauswahl erstellen
- Lieferantenqualifizierung vornehmen
- Lieferantenauswahl treffen
- Lieferantenüberwachung etablieren
- Lieferantenauswahl
- Lieferantenüberwachung
Ausgelagerte Prozesse in der Medizintechnik